הרצאה 2 - מבנה החלבון
רמות המבנה של חלבון:
-
מבנה ראשוני:
- קשר פפטידי של מספר חומצות אמינו (נבנה בריבוזום)
-
מבנה שניוני:
- צורת הקיפול של החלבון: אלפא הליקס או בטא שיטס (חלבון יכול להכיל גם וגם). נקבע לפי השיירים החופשיים שבהם מידע שמכווין את הקיפול.
- אלפא הליקס:
- מחוזק ע"י קשרי מימן
- קשרי מימן נוצרים בין החמצן של קצה קרבוקסילי למימן בקצה האמיני של החומצה הרביעית שאחריו
- סיבוב אחד של הסליל = 3.6 חומצות אמינו
- אורך סיבוב אחד = 5.4 אנגסטרם
- בטא שיטס:
- מבנה דמוי זיג זג המיוצב על ידי קשרי מימן בין הסיבים, מתחלק לשני סוגים:
- מקבילי - parallel:
- השיריים נמצאים באלכסון ורחוקים יותר אחד מהשני בהשוואה לאנטי מקבילי
- החיבור נעשה תמיד מהקצה האמיני לקרבוקסילי - המשטחים מחוברים עם לופים (ארוכים יותר מבטא טורנס)
- לדוגמא:
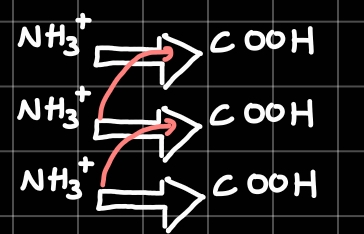
- אנטי מקבילי - Anti parallel:
- השיירים שיוצרים את קשרי המימן מסודרים יותר ולכן המבנה יותר חזק ויציב
- החיבור בין הקצה האמיני לקרבוקסילי מתבצע באמצעות בטא טורנס
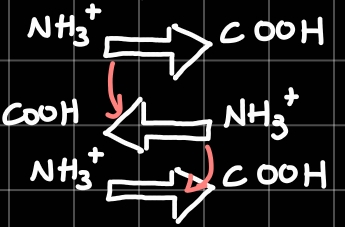
- מקבילי - parallel:
- מבנה דמוי זיג זג המיוצב על ידי קשרי מימן בין הסיבים, מתחלק לשני סוגים:
-
מבנה שלישוני:
- קיפול תלת מימדי של פולי - פפטיד, על ידי קשרים דיסולפידים (ציסטאין).
- מתחלק לשתי קבוצות עיקריות של חלבונים:
- פקעתיים:
- חלבונים גלובולרים, שרשראות פולי פפטידיות שיוצרים צורה גלובולרית
- מסיסים במים
- סיביים:
- חלבונים סיביים, שרשראות פוליפפטידיות שיוצרות רצועות ארוכות
- לא מסיסות במים
- פקעתיים:
-
מבנה רבעוני:
- קשר בין מספר יחידות
דנטורציה:
- איבוד המבנה המרחבי של החלבון, שגורם לאיבוד הפונקציה
- גורמים לדנטורציה:
- חום: משפיע על אינטרקציות חלשות כמו קשרי מימן
- שינוי ממסים: כגון אוריאה (urea) שמשנים את הערכות קשרי המימן
- ריאגנטים מחזרים: אשר שוברים את קשרי ה S-S (קשרים דיסולפידים אשר נוצרים באמצעות ציסטאין)
- ערך PH קיצוני
- ניסוי אניפנסן:
- אנפינסן גילה שאם לוקחים חלבון שעובר דנטורציה, וקודם מוציאים את האוריאה ורק אז מחמצנים (ביטול השפעת ריאגנט מחזר), אפשר לגרום לרנטורציה ב- 90%.
- לעומת זאת, סדר פעולות הפוך (חמצון ואז הוצאת האוריאה) גורמת ליצירה רנדומלית של קשרים דיסולפידים ולכן לא יתקבל מבנה נכון, רמת הרנטורציה תהיה 1-2%
שיטות ריצוף חלבון:
- ריאגנט סנגר:
- ריאגנט שנקשר לקצה האמיני של החומצה הראשונה בשרשרת. ניתן להוסיף HCL שמפרק את כל הקשרים הפפטידים וכך יותר קל לזהות את החומצה הראשונה שמחוברת לריאגנט.
-
ריאגנט אדמן:
- פעולה דומה לריאגנט סנגר. ההבדל הוא שריאגנט אדמן מפרק את החומצה הראשונה בעצמו. כך אפשר להשתמש בו שוב ושוב כדי לרצף את החלבון
- אפקטיביות הריאגנט פוסקת לאחר בערך 30 חומצות אמינו
-
פרוטאזות:
- אנזימים שמפרקים קשרים פפטידים:
- טריפסין (Trypsin): חותך אחרי Lys או Arg
- כימוטריפסין (chymotrypsin): חותך אחרי Trp , Phe או Tyr
- פפסין (pepsin): חיתוך לפני Phe
- ציאנוגן ברומיד (cyanogen bromid): חיתוך אחרי Met
- הפירוק של פפטידים ארוכים לכמה פפטידים קצרים אומר שנוכל להשתמש בריאגנט אדמן
- אנזימים שמפרקים קשרים פפטידים:
-
ספקטרומטריות מסה:
- חותכים חלבון למספר פפטידים ומייננים אותם. את הפפטידים המיוננים מאיצים במכשיר במעל מגנט
- פפטידים בעלי מסה גבוהה יותר קיבלו יותר מטען ולכן לא יוסטו ממסלולם באמצעות המגנט
- נוצר מצב שבו לכל פפטיד במסה שונה יש מסלול משלו וכך ניתן לרצף כמה מכל פפטיד היה בחלבון
-
דף sds:
- שיטה נוספת לחלוקה לפי מסה
- לאחר דנטורציה, מולקולות של sds (טעון שלילית) מתחברות לחלבונים.
- את החלבונים שמים בג'ל שטעון חיובית בקצה אחד ושלילית בשני
- המולקולות הארוכות יותר (יותר מסה) יעברו ביותר קושי בג'ל ויקח להם יותר זמן להגיע לקצה. מכך נוצרת הפרדה לפי מסה (נקרא גם Bands)
- גם אם יש מוטציה בחלבון, כל עוד החלבון נשאר בערך באותו משקל (בין אם חומצת האמינו שהוחלפה היא באותו משקל או שכמות החומצות שהוחלפו היא זניחה), ה Band ישאר באותו מקום.